05404 KI in der Genomsequenzierung während neurochirurgischer Operationen
|
Künstliche Intelligenz (KI) kann Ärzten im Krankenhaus in vieler Hinsicht helfen – dieser Beitrag stellt vor, wie KI bei der klinischen Entscheidungsunterstützung im OP zum Einsatz kommen kann. von: |
Tumore des Zentralnervensystems sind eine der tödlichsten Krebsarten, insbesondere wenn diese bei Kindern auftreten. Die Primärbehandlung umfasst die neurochirurgische Entfernung des Tumors während eines intraoperativen Eingriffs. Die Herausforderung dabei ist, dass ein empfindliches Gleichgewicht zwischen der Maximierung des zu entfernenden Tumorgewebes und der Minimierung des Risikos neurologischer Schäden und Komorbiditäten gefunden werden muss.
Chirurgen und Neurochirurgen haben vor der Operation jedoch nur begrenzte Kenntnisse über die genaue Tumorart. Die derzeitige Standardpraxis stützt sich auf die präoperative Bildgebung und die intraoperative histologische Analyse (sogenannter Schnellschnitt während des operativen Eingriffs), die jedoch nicht immer schlüssig und gelegentlich falsch sind.
Nanoporen-Sequenzierung
Mittels schneller Nanoporen-Sequenzierung kann während einer neurochirurgischen Operation ein spärliches Methylierungsprofil erhalten werden. Der Begriff DNA-Methylierungsprofil stammt aus dem Fachgebiet der translationalen Onkologie und der Epigenetik und bezeichnet diagnostische und prädikative Marker aus der Genomsequenzierung. Im Gegensatz zur Genetik, die den Bauplan für die Erbinformationen in der DNA kodiert, regelt die Epigenetik die Nutzung dieser Informationen. So ist es möglich, dass Zellen im Körper unterschiedlichste Funktionen erfüllen können, obwohl sie in der Regel die identischen Chromosomensätze besitzen.
Mittels schneller Nanoporen-Sequenzierung kann während einer neurochirurgischen Operation ein spärliches Methylierungsprofil erhalten werden. Der Begriff DNA-Methylierungsprofil stammt aus dem Fachgebiet der translationalen Onkologie und der Epigenetik und bezeichnet diagnostische und prädikative Marker aus der Genomsequenzierung. Im Gegensatz zur Genetik, die den Bauplan für die Erbinformationen in der DNA kodiert, regelt die Epigenetik die Nutzung dieser Informationen. So ist es möglich, dass Zellen im Körper unterschiedlichste Funktionen erfüllen können, obwohl sie in der Regel die identischen Chromosomensätze besitzen.
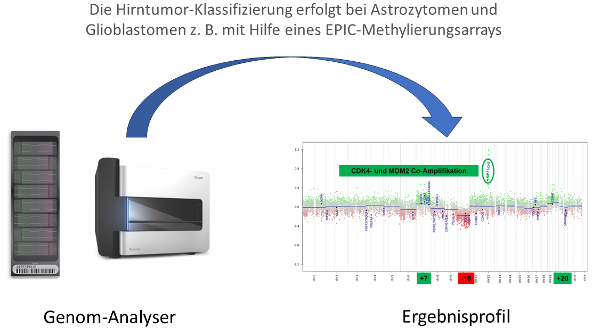
Epigenetische Mechanismen beschreiben die an Tochterzellen mitotisch und meiotisch vererbbaren Veränderungen in der Genfunktion, die nicht aus einer DNA-Sequenzveränderung resultieren. Sie wirken z. B. über DNA-Methylierung. Abbildung 1 stellt vereinfacht einen Analyser aus der Epigenetik mit einem dazugehörigen Bildbefund dar.
Abb. 1: Illumina Chip und iScan System (Courtesy of Illumina, Inc.)
Labortechnische Arbeitsumgebung
Mithilfe der EPIC-Diagnostik können Gehirntumore anhand von Biopsiematerial über die Bestimmung der epigenetischen Tumorsignaturen (DNA-Methylierungsprofil) sowie die Anwendung maschineller Algorithmen (Brain Tumor Classifier) über den Vergleich mit einer Referenzgruppe von über 2.800 Hirntumoren prognostisch und therapeutisch wichtigen Tumorentitäten bzw. Risikogruppen zugeordnet werden (sogenannte EPIC Diagnostik/kindliche Hirntumor-Classifier).
Mithilfe der EPIC-Diagnostik können Gehirntumore anhand von Biopsiematerial über die Bestimmung der epigenetischen Tumorsignaturen (DNA-Methylierungsprofil) sowie die Anwendung maschineller Algorithmen (Brain Tumor Classifier) über den Vergleich mit einer Referenzgruppe von über 2.800 Hirntumoren prognostisch und therapeutisch wichtigen Tumorentitäten bzw. Risikogruppen zugeordnet werden (sogenannte EPIC Diagnostik/kindliche Hirntumor-Classifier).
OP-Saal-Umgebung
Neurochirugische Operationen werden in speziell ausgestatteten OP-Sälen durchgeführt (Beispiel Klinikum Stuttgart). Zur Ausstattung gehören:
Neurochirugische Operationen werden in speziell ausgestatteten OP-Sälen durchgeführt (Beispiel Klinikum Stuttgart). Zur Ausstattung gehören:
| • | OP-Tisch mit Neurochirurgiezubehör, z. B. spezielle Kopfkalotte oder Mayfield-Halterung |
| • | OP-Mikroskop Neurochirurgie |
| • | OP-Navigation (Qualitätssicherung) |
| • | OP-Bildbetrachungsmonitore (intraoperative Sicht und PACS) |
| • | spezielles neurochirurgisches OP-Instrumentarium |
Alle medizinischen Geräte sind in einem medizinischen IT-Netzwerk (MIT) vernetzt. Pathologische Befundergebnisse, zum Beispiel nach einem Schnellschnitt, können über das MIT auf einem Großbildmonitor eingeblendet werden.
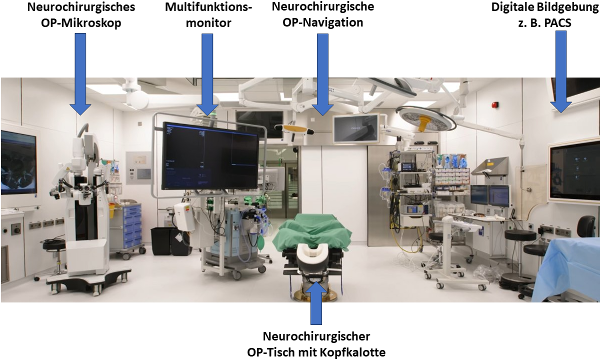
Abbildung 2 zeigt eine typische Ausstattung eines OP-Saals mit der Spezialisierung auf neurochirurgische Eingriffe.
Abb. 2: Neurochirurgischer OP-Saal
Aufgabe der KI ist es, anhand der Methylierungsdaten für jede Tumorgruppe einen möglichst unverwechselbaren Fingerabdruck zu identifizieren, um damit die Diagnose zu verfeinern (siehe auch News des Uni-Klinikums Heidelberg).
Molekulare Subklassifizierung von Tumoren
Für die patientennahe schnelle Tumordiagnostik wurde durch ein Team des Oncode Instituts in Utrecht Sturgeon entwickelt, ein patientenunabhängiges neuronales Netzwerk mit Transfer Learning, um eine molekulare Subklassifizierung von Tumoren des Zentralnervensystems auf der Grundlage spärlicher Profile zu ermöglichen. Sturgeon lieferte innerhalb von 40 Minuten nach Beginn der Sequenzierung in 45 von 50 retrospektiv sequenzierten Proben eine genaue Diagnose (Verzicht auf die Diagnose der anderen fünf Proben). Darüber hinaus wurde die Anwendbarkeit in Echtzeit während 25 Operationen demonstriert und eine diagnostische Durchlaufzeit von weniger als 90 Minuten erreicht. Davon waren 18 (72 %) Diagnosen korrekt und sieben erreichten nicht die erforderliche Konfidenzschwelle.
Für die patientennahe schnelle Tumordiagnostik wurde durch ein Team des Oncode Instituts in Utrecht Sturgeon entwickelt, ein patientenunabhängiges neuronales Netzwerk mit Transfer Learning, um eine molekulare Subklassifizierung von Tumoren des Zentralnervensystems auf der Grundlage spärlicher Profile zu ermöglichen. Sturgeon lieferte innerhalb von 40 Minuten nach Beginn der Sequenzierung in 45 von 50 retrospektiv sequenzierten Proben eine genaue Diagnose (Verzicht auf die Diagnose der anderen fünf Proben). Darüber hinaus wurde die Anwendbarkeit in Echtzeit während 25 Operationen demonstriert und eine diagnostische Durchlaufzeit von weniger als 90 Minuten erreicht. Davon waren 18 (72 %) Diagnosen korrekt und sieben erreichten nicht die erforderliche Konfidenzschwelle.
Es wird die Schlussfolgerung gezogen, dass eine maschinell auf einem KI-Algorithmus erlernte Diagnose auf der Grundlage kostengünstiger intraoperativer Sequenzierung die neurochirurgische Entscheidungsfindung (klinische Entscheidungsunterstützung im OP) unterstützen kann, wodurch möglicherweise neurologische Komorbiditäten verhindert und zusätzliche Operationen vermieden werden können.
Weitere Informationen:
| • | Vermeulen, C., Pagès-Gallego, M., Kester, L. et al. Ultra-fast deep-learned CNS tumour classification during surgery. Nature 622, 842–849 (2023). |
| • | Oxford Nanopore Technologies: qcat |